細胞内PPI阻害を可能にするin silico中分子設計技術の開発
情報理工学院 情報工学系 助教 大上 雅史
医薬品研究開発において近年タンパク質間相互作用 (protein-protein interaction, PPI) を標的とする阻害薬の開発が注目されています。現在のPPI阻害薬は抗体医薬などの高分子医薬品が主流となっていますが、高分子医薬品が標的とするのは主に細胞表面の膜タンパク質です。これは、高分子医薬品が細胞膜を通過して細胞の中に入ること=細胞膜透過がきわめて難しいことによります。細胞表面だけではない細胞内の多くのタンパク質が関わるPPIの阻害を可能にするためには、医薬品が細胞膜透過できることが必須となります。また、細胞内にはまだまだ未知のPPIが多数存在しており、それら知られざるタンパク質同士の関係が、どの標的分子を狙って医薬品開発を進めるか、未知の副作用の可能性はないかといった医薬品開発における重要な道標となります。
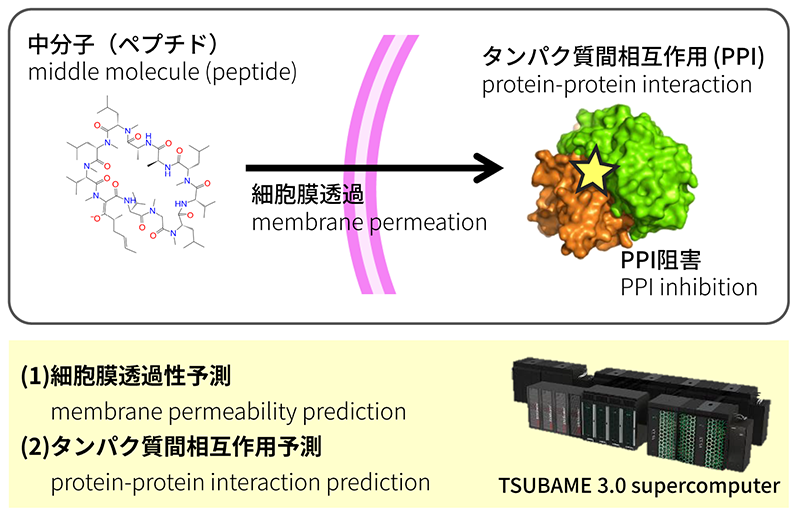
私たちは、これまでに計算=in silicoによる分子設計技術・創薬支援技術の開発に取り組んできました。特に、ペプチド等の中分子化合物の細胞膜透過性を計算機で予測する技術、およびは細胞内の未知PPIを計算機で網羅的に予測する技術により、細胞内PPI阻害を可能にする中分子化合物設計を進めています。
中分子化合物はその名のとおり高分子医薬品と低分子医薬品の中間的な大きさですが、高分子のように高いPPI阻害能が期待され、また低分子のように細胞膜透過性も良いことが知られています。しかしながら、どんな中分子でも細胞膜透過ができるわけではなく、わずかな構造の差異でも細胞膜透過性が極端に変化することがわかっています。どのような分子が細胞膜透過能を有するかは、実際に生物学的実験で試してみないとわからない状況でした。私たちは、東工大TSUBAME 3.0スーパーコンピューターを駆使した計算機による分子シミュレーション技術と、機械学習技術を組合せることで、従来の10万倍高速な計算パイプラインを構築し、中分子化合物の細胞膜透過性を計算によって予測できるようなシステム開発を進めています。
また私たちが開発したPPIの網羅的予測の技術は、TSUBAME 3.0を高効率に利用する実装により、100万通りのタンパク質同士の組合せでもわずか半日程度でPPIを予測することができます。これらの計算技術により、細胞内PPI阻害が可能な中分子化合物の設計を強力に推し進めていきます。
お問い合わせ先
東京工業大学 研究・産学連携本部
E-mail:sangaku[at]sangaku.titech.ac.jp